Vederi moderne cu privire la geneza și tratamentul șocului durerii. Shock ca pierdere acută de sânge masive
Shock ca pierdere acută de sânge masive
Chirurgie si traumatologie, în mod constant întâlni în practica lor cu echimoze interne extinse și sângerare, cum este experiența dobândită empiric la concluzia că șocul - este în primul rând o pierdere acută de sânge masive.Se arată că bine-cunoscutele modele experimentale de șoc B. Cannon, când este numit de mai multe ori cu un obiect de metal greu pe extremitățile matrice de țesut de animale, ceea ce duce rol patogenic este jucat de asemenea hemoragie [Nasonkin O. Din 1984].
Teoria de sânge și plasmă a fost cea mai fructuoase pentru dezvoltarea unui tratament eficient al șocului traumatic.
medic În primul rând, este orientat corect pentru a căuta rapid sursa de sângerare ca o cauza rădăcină de șoc, și în al doilea rând, un rol crucial în tratamentul hemostaza pe perioadă determinată retrogradat și refinanțarea adecvată a pierderii de sânge. Cea mai recentă etapă în studiul problemelor de șoc a început în 60 de ani ai acestui secol și a avut loc concomitent cu dezvoltarea și stabilirea de resuscitare. În a fost creat unele orașe mari ale țării noastre și centre antișoc în străinătate de rețea, destinat tratamentului intensiv de leziuni grave.
cercetare clinico-fiziologice a fost efectuată în mod direct la masa de operație, la patul în ICU. În același timp progresele tehnologice permit o mai mare adâncime de monitorizare starea funcțională a principalelor sisteme funcționale (de monitorizare), iar rezultatele sunt prelucrate cu ajutorul calculatoarelor. Ca urmare, datele au fost obținute prin modificarea opiniilor tradiționale de șoc traumatic ca un proces reflex pur neuromusculare.
Analiza unui număr mare de observații au arătat că diagnosticul „șoc“, ori de câte ori apare în practica clinică, când a înregistrat scăderea tensiunii arteriale. Între timp, cauza imediată a hipotensiunii răni grave poate fi pierderea acută de sânge, daune directe suferite de organe vitale, hipoxie profundă și acidoză, intoxicație. Acțiunea acestor factori de fiecare dată când se desfășoară pe fondul unor impulsuri și reacții tipice neuroendocrine (stres) patologice.
Cu toate acestea, rolul specific al ultimelor consecințe patologice considerabil mai puține pierderi directe de volume mari de sânge, opriți funcțiile specifice de organe vitale sau alte complicații traume imediate. șoc traumatic gradul III, în 75% din toate cazurile însoțite de deficit bcc, egală cu 30% sau mai mult, în timp ce se află în stare terminală pierderi de sânge masive înregistrate în 33% din cazuri [Egurnov NI, 1970].
Deși corelația dintre severitatea șocului (nivelul tensiunii arteriale) și valoarea pierderii de sânge este foarte aproape, dar nu se ajunge la o valoare de 100%. Prin urmare, pierderea acută de sânge nu este întotdeauna responsabil pentru dezvoltarea de dezastru hemodinamic (soc) in leziuni grave. De exemplu, dacă pagube, vătămare strivire, dezlipire de separare a pielii și completă a membrelor, în plus față de pierderea de sânge, exprimat în mare măsură rolul patogenic de intoxicare.
Studiul endotoxemiei traumatizant a fost pus la începutul acestui secol, atunci când se utilizează injecția histamină la animalele experimentale care au primit hipotensiune arterială prelungită. După sfârșitul celui de al doilea război mondial a fost chiar formulat teoria șocului traumatic toxic [Kenyu, Delbo 1919]. Din practica clinică, este bine cunoscut faptul că leziunile masive și fluxul de sânge distrugere a membrelor nu poate fi normalizat atâta timp cât nu va fi amputat strivire segment tratat rana, replantate pielea pe rana tratata impus pansament aseptic protector.
În compoziția substanțelor care circulă posedă influențe intoxicației detectate amine toxice (histamină, serotonină) și polipeptide (bradikinină, kallidin), prostaglandine, enzime (enzime lizozomale), metaboliți tisulare (acid lactic, electroliti, compus adenina, feritinei). Toate aceste substanțe au un efect inhibitor direct asupra hemodinamicii, schimbul de gaze și, prin aceasta exacerba manifestările clinice ale șocului. Ei încalcă barierele antimicrobiene, contribuie la formarea de efecte ireversibile ale șocului.
În prezentarea patogeneza șocului, nu putem ignora conceptul de insuficiență multiplă de organe (MODS), câștigă o mulțime de popularitate. OPA - este răspunsul organismului Biosystems la agresiuni severe (șoc, sepsis, etc.). Cel mai probabil nu este direct legată de cele de mai sus, și la un nivel mai subtil, explică motivele pentru moartea pacienților privați de îngrijire adecvate. Cu toate acestea, aceste încălcări sunt mai specifice pentru etapele ulterioare de șoc, medicul trebuie să știe. Principalele prevederi ale conceptelor OPA sunt după cum urmează.
Celulele endoteliale vasculare nu sunt căptușeală pasivă. Când vazimodeystvii cu catecolamine acestea dau un impuls elementele celulare ale sângelui, ceea ce duce la o creștere a adezivității, agregare, degradare, deteriorarea proprietăților reologice ale sângelui. Celulele endoteliale Excited produc vase factor de relaxare - acțiune rapidă substanță cu un timp de înjumătățire de 1 minut și substanța care acționează lent cu efectul opus.
Formată în această agresiune mediatori au fost mult mai activi decât substanțele biologice menționate mai sus din grupul aminelor. Acești mediatori sunt împărțite în mai multe grupe: eicosanoizi (tromboxani, leucotriene, prostaglandine), care acționează asupra microcirculației, hemostaza, permeabilitatea membranei și netede citokine ORGANE musculare - proteine, peptide produse de fagocitele și limfocite.
au fost deschise trei citokine: fibronectina, celule endoteliale capabile de clei și le fixa pe membrana bazală, substante de purificare a sângelui din natură acelular și accelera limfokine ran- plăgilor, rezultând într-un exces de limfocite cu orice agresiune antigenică, declanșează un răspuns autoimun, însoțită de pierderea cașectină kletok- produsă de macrofage activează neutrofilele, stimulează eliberarea de substanțe biologic active, modifică activitatea T și B-limfocite afecteaza perfuziei tisulare determina clinica septic Skogen șoc.
Ca rezultat, agresiunea a produs peptide cu greutate moleculară 1000- 10000 și „molecule de mijloc“, care, la rândul său, crește permeabilitatea membranelor și perturbă oxidarea microcirculației normale, sinteza ADN-ului, hematopoieză. Numărul de molecule „de mijloc“ se corelează cu severitatea stării critice. Orice agresiune însoțită de activarea oxidării radicalilor liberi și peroxidarea. Cu toate acestea, dintr-un exces de radicali liberi împiedică sistemul antioxidant - catalaza, superoxid dismutaza.
Hipoxia și alte tipuri de agresiune, oferi un stimulent pentru oxidarea radicalilor liberi generalizată, care nu este în măsură să „facă“ sistemului antioxidant. Peroxidarea lipidică duce la formarea unei cantități mari de acizi grași nesaturați cu efect dăunător mai puternic asupra membranelor celulare, organitelor surfactant.
Astfel de enzime, proteine inactivate cu grupări sulfhidril. polizaharide simultan depolimerizată constituind matriks- intercelulare deteriorate ADN. In general, activarea oxidării radicalilor liberi destabilizează membranele crește permeabilitatea și conduce la formarea de Fe2 + și întreruperea producției de energie.
Aceste procese au loc în toate organele și țesuturile, diferențele observate în rata și amploarea daunelor cauzate de caracteristicile circulatorii în ele. De exemplu, creier și sânge ale vaselor inimii au, în general, în sistem adrenergice și eliberarea de catecolamine reacționează prosveta- crește fluxul de sânge în piele și rinichi suferă atât în stadiile incipiente ale stării critice.
Manifestarea clinică a OPA folosind două etape. Primul schimb de gaze este perturbat, sistemul hemostatic, numărul de trombocite din sânge se reduce, valori crescute ale bilirubinei, enzime (ACT, ALT și altele.). tulburări neurohumorale provoca tulburări circulatorii, pregătirea „terenului“ pentru dezvoltarea insuficienta pulmonare, renale și hepatice, precum și pentru apariția ulcerului stres tractului gastrointestinal. În faza târzie a OPA (decompensare), format la schimbările ireversibile la nivel subcelular, ca urmare a mitocondriilor insuficienta funcționale progresive atunci când energia începe să „digere“ aminoacizi în loc de carbohidrați.
Din această cauză, inhibă sinteza proteinelor, enzime, imunoglobuline, factori de coagulare. Ca urmare, a încălcat funcția de barieră a stomacului și a pereților intestinali, iau trombocitopenie, hiperglicemie, insuficiență cardiacă, disfuncție a altor organe.
Mai exact, OPA este compus din următoarele sindroame:
- ARDS: (lipsă de aer mai mult de 36 de respirații pe 1 min), hipoxemie (PaO2 < 50 мм рт. ст.), измененные соотношения РаО2/FО2
(< 200), комплайнс-теста (35 мл/см вод. ст.), необходимость многочасовой ИВЛ в режиме ПДКВ;
- AKI: oligurie (ieșire urină 500 ml / zi sau mai puțin), niveluri crescute ale creatininei serice (mai mare de 0,15 mmol / l), creșterea concentrației de sodiu în urină (40 mmol / l), raportul dintre osmolalitatea urinei modificat și plasmă (mai puțin de 1, 2);
- OPech H: creșterea cantității de bilirubină în sânge (mai mult de 75,5 mmol / l), a redus concentrația de albumină (mai puțin de 30 g / l), hiperglicemie persistentă;
- DIC: trombocitopenie (100000 / mm3 sau mai puțin), reducerea timpului de protrombină și protrombinei parțială, hipofibrinogenemie, prezența în sânge a produselor de degradare a fibrinei;
- insuficiență cardiacă acută: hipotensiune arterială (mai mică de 90 mm Hg ..), o scădere a indicelui cardiac (mai puțin de 1,5 L / min-m2), și munca de accident vascular cerebral a ventriculului stâng (mai mic de 35), creșterea "presiunii pană" (20 mm Hg; Art.), aritmie ventriculară .;
- tulburări ale tractului gastrointestinal: pareze, cu descărcare a conținutului prin tubul nasogastric într-o cantitate mai mare de 1 l / d, ulcerații ale mucoasei gastrice și duodenale mucoasei (endoscopice);
- tulburări funcționale ale sistemului nervos central: sedare, comă, psihoză acută.
Mortalitatea în OPA este determinată de doi factori majori: numărul de organe sau sisteme afectate și datele la începutul terapiei intensive. Odată cu înfrângerea unui sistem funcțional leta- > lnost este de 13%, două - 34%, trei - 80%, patru - 93%, cinci sau mai multe - 100%. Tratamentul PON cu succes atunci când se bazează pe principiile de terapie intensivă și are o prevenire activă în natură.
In practica clinica pentru diagnosticul de „șoc“, este de multe ori se află diferite stări critice, termenul dobândește adesea un sens colectiv. În această interpretare, diagnosticul de șoc are nevoie de o interpretare detaliată a unei liste specifice a tuturor leziunilor și este strâns legată de tulburări funcționale.
Cu toate acestea, influența dominantă a pierderii acute de sânge din cauza deteriorării mecanice dă motive să ia în considerare șocul traumatic în primul rând ca sindromul gipotsirkulyatsii. Principalele efecte patofiziologice ale pierderii acute de sânge este o reducere masivă a bcc (hipovolemie), reducerea fluxului sanguin la nivelul inimii și astfel la scăderea productivității, creșterea tonusului vascular periferic. Gradul de hipovolemie - condițional capacitate de neadaptare volumul patului vascular rămânând în linia circulației sângelui - judecat indirect de amploarea pierderii de sânge, scăderea fluxului sanguin venos la nivelul inimii si reducerea debitului cardiac (IOC).
Reducerea acută bcc 20% este considerat ca nivelul critic la care IOC este redus la jumătate, și conservate fluxul sanguin nu se mai poate asigura perfuzie adecvată a țesutului, excreția metaboliților deșeurilor.
perfuziei tisulare redusă la prima etapă interferează cu funcția de organe și sisteme, pe al doilea - provoacă modificări morfologice ale structurilor celulare. Starea de hipovolemie și șoc poate provoca plazmopoterya acută (cu detașare extensivă, inflamație intensă), deshidratare semnificativă, pierderea de sare (vărsături, prin fistule). În stadiile incipiente este dificil să-i spuneți diferența dintre aceste specii de șoc hipovolemic (cauzate de pierderea de sânge sau pierderea de plasmă), ca și pentru fiecare dintre ele caracterizate printr-un tablou clinic de „tahicardie hipotonă rece“.
Dinamica șoc obișnuiește să se facă distincția stadiu timpuriu cu răspuns compensator marcat. Acesta este caracterizat prin reacția circulatorii hyperdynamic prin acțiunea mecanismelor de compensare debitului volumetric IOC este menținut la un nivel ridicat. Cu o ușoară scădere a tensiunii arteriale sau a unei creșteri de nivel normale parametrii hemodinamici de bază: frecvență cardiacă, K0, debitul cardiac, CSC, cardiace, livrarea de oxigen la nivelul tesuturilor.
Dezvoltarea spasm vascular periferic, creșterea OPS marcant și a consumului de oxigen tisular. Prin urmare, creșterea diferenței A-B și gradul de saturare cu oxigen a oxigenului periferic la nivelul țesuturilor. Rezultatul acestor modificari compensatorii este o digestie mai completă a țesuturilor oxigen. În stadiile incipiente activeaza sistemul nervos simpatic.
spasm generalizat al vaselor periferice
În termen de 30-60 secunde dupa trauma si pierderea de sange se produce spasm generalizat periferic răsadurile vascular ca legătură de sânge ( „rezistența sistem“), iar vasele venoase de diametru mic ( „sistem capacitiv“). vasoconstricție pe scară largă contribuie la producerea și eliberarea de catecolamine în sânge a crescut - principalii hormoni suprarenali (epinefrină, norepinefrină).Stimulente pentru sporirea activității de circulație și de schimb de gaze a fost primit de la mari centre autonome ale trunchiului cerebral. În direcția stimulării sunt de asemenea produse de celule deteriorate, tulburări metabolice, sisteme de chinină substante si alte tulburari endotoxine microcirculație.
Cu toate acestea, nu toate zonele navelor sunt reduse în mod egal. Pentru un grad mult mai mare de vasoconstricție se aplică pe piele, țesutul adipos subcutanat, mușchi scheletic, organe interne zona splanchnic, care au o importanță vitală într-o situație de urgență.
Ca urmare a spasmului sanguin vascular periferic este mobilizat în părțile centrale ale patului vascular, oferind perfuzia organului primar, deosebit de sensibile la hipoxie, inimă, creier (reacție "centralizare circulator") Și adverse rezultatul este stocat până la dezvoltarea fazelor de șoc terminale.
Acesta definește vasoconstructie simptomele cele mai izbitoare de șoc: paloarea pielii și a mucoaselor, picături mari de sudoare rece lipicios. Se lasă amprenta pe parcursul perioadei post-traumatic (insuficiență renală acută, enterită hemoragică). vasospasm inegala la diferite regiuni anatomice și determină un număr inegal de receptori care sunt sensibile la adrenalina si noradrenalina. Deoarece acești receptori este mai puțin probabil în creier și inimă, alimentarea cu sange scade ultima. Există, de asemenea, propriile sale mecanisme de autoreglare a alimentarii cu sange a acestor organe care îndeplinesc funcții vitale.
Având în vedere creșterea consumului de oxigen de tesuturi si energie, impreuna cu hemodinamică stimuleaza toate procesele de schimb de gaze. Scurtarea respirației și creșterea alocării pierderii drept cu C02 rezerve alcaline (hemoragie) cauza hipocapnia și alcaloză. În cazul în care mediile normale de consum de oxigen 80 ml / (min * m 2), după daune grele crește aproape 2 ori [150 ml / (min * m 2)].
Pentru a compensa nevoile tot mai mari ale țesuturilor pentru materiale plastice si oxigen, protejeaza celulele de la daune a crescut rata volumului krovotoka- „centralizarea circulației“, iar în acest caz, joacă un rol important. Ca urmare a acțiunii unor mecanisme compensatorii hemoragie, ajungând la 10-15% din CCA, aceasta este însoțită de tulburări hemodinamice minime.
Pierderea de sânge în cantitate de 20 30% BCC poate fi deplasat în mod independent de către organism fără sânge semnificativ pierderea de sânge de scădere a presiunii într-o cantitate de 30-50% bcc provoacă hipotensiune arterială profundă care necesită tratament energic de urgență pentru salvarea pacientului.
În condiții strangeti giportsirkulyatsii și dezoxigenarea continuă metabolismului celular pentru generarea de energie electrică cale anoxic (glicoliza anaerobă). Aceasta definește esența principiului proceselor patologice în al doilea (tardiv) șoc etapă numită „faza decompensare“. natura patogenetic stadiu tardiv în celule este determinată de schimb încălcare.
rol important în mecanismul de tulburări fiziopatologice aparține acidoză metabolică, care are loc în organism datorită acumulării de acid lactic și a altor produse acide deranjat metabolismul, influențează în mod activ funcția multor organe și sisteme. În particular, acidoza stimulează funcția medulosuprarenalei și echilibrul dă electroliții de bază potasiu ioni părăsesc și ionii de sodiu sunt transferate în celule (celule transmineralizatsiya).
Procesul transmineralizatsii duce la creșterea volumului intravascular și este, de asemenea, drept scop menținerea CCA. Rezervele intracelulară de compuși ai fosforului - principalii purtători de energie - sunt epuizate rapid. Creșterea nivelului de adrenalină în sânge este asociată cu creșterea descompunerea glicogenului în ficat, hiperglicemie si impiedicat de glucoza primirea in celule ( „mellitus traumatice“).
În leziuni grave, însoțite de hipotensiune arterială prelungită, hipovolemie profundă și picătură în funcția de pompare a inimii, dezvolta tulburări ale microcirculației, care este considerată pe bună dreptate unificatoare sindroamele de șoc cadru de origine diferită. Cu debutul spasm vascular perfuzia țesuturilor periferice este redus drastic (până la 1 L / min).
Ca răspuns la această reducere sunt dezvăluite anastomozele arteriovenoase ocolite (șunturi) și volumul crește perfuzie din nou la un nivel normal (4 litri / min). Cu toate acestea, rata fluxului sanguin periferic a încetinit brusc, iar această decelerare în zona „arteriolelor - capilare - venule“ devine ireversibil. În dinamica tulburărilor microcirculatorii sunt clar vizibile trei faze.
In prima faza a redus sfinctere pre- și post-capilare și în cele mai multe zone ale țesutului nu mai primesc sânge (anoxia ischemic). In faza a 2, sfinctere precapilare relaxa și postcapilare încă spasmatic (stază capilară). În a treia fază pre rasslablyayutsa și sfinctere post-capilare, dar gradientul de presiune nu mai este suficient pentru a restabili perfuzia țesuturilor periferice (pareze vasculare periferice).
Deși capilare funcționale normale conțin 5% din CCA, iar la înălțimea tulburărilor microcirculatorii 25% CCA, fluxul sanguin de țesuturi nu este restabilit, iar apoi efectul deplin manifestata de hipoxie. Cultivarea tulburare circulatorie periferică, eventual, duce la o încetare completă a fluxului sanguin la locul „capilar venule“, ceea ce determină o creștere a presiunii capilare, îmbunătățită filtrarea partea lichida a sangelui care curge în spațiul extracelular. sânge vâscozitate crescută, dezvoltarea sindromului CID.
Odată cu aprofundarea hipoxie și acidoză deteriorat structura internă a celulelor, ruperea membranei de lizozomi, în canalul de circulație primește enzime (fosfataza acidă, a-glucuronidaza). In timp ce hipoxie afectează în mod egal toate țesuturile, diferite organe nu sunt la fel de sensibile la acesta.
De exemplu, mucoasa tractului gastrointestinal este deosebit de lizozomi bogate, care, în condiții de hipoxie și inundă corpul sfâșiat de substanțe toxice și inhibarea funcției hepatice previne a le neutraliza. Ca rezultat, care circulă în proteaza sânge, amine biogene, peptide vasoactive, prostaglandine aprofunda în continuare a crizei microcirculatiei și încălcarea funcțiilor organelor și sistemelor.
Hipotensiunea sub 80 mmHg. Art. încalcă perfuzia sanguină a stratului cortical de rinichi, producția de urină încetează. Activitatea cardiacă se deteriorează sub influența hipovolemiei, reducerea fluxului sanguin venos la nivelul inimii, acidoză în creștere, tulburări de reologie sânge.
În plus, condițiile de pierdere de sânge, pierderea directă a hemoglobinei, crescand cerintele de tesut de oxigen sunt creșterea fluxului sanguin la cerințele organe și țesuturi. Când hipoxie, acidoză deranjat puternic funcției pulmonare: există un vasospasm, circulația pulmonară, permeabilitate capilară crescută pulmonară, edem crește legkih- din cauza blocarea vaselor mici de sânge microtromboză alveolele nu mai sunt alimentate cu sânge.
Ca rezultat al distribuirii sângelui depreciat, în creștere deficit în aprovizionarea cu oxigen a țesuturilor și a acumulării de substanțe toxice din organism apar modificări profunde homeostaziei, iar apoi vine distrugerea structurilor celulare (etapa finală ireversibil, sau refractar, șoc).
VN Tsibulyak, GN Tsibulyak
Distribuiți pe rețelele sociale:
înrudit
 Primul ajutor pentru șoc
Primul ajutor pentru șoc Primul ajutor pentru sângerare din gura
Primul ajutor pentru sângerare din gura Primul ajutor pentru sângerare. tipuri de sângerare
Primul ajutor pentru sângerare. tipuri de sângerare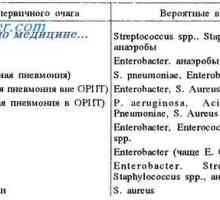 Șoc septic. Cauzele și mecanismele de dezvoltare a șocului septic
Șoc septic. Cauzele și mecanismele de dezvoltare a șocului septic Vederi moderne cu privire la geneza și tratamentul șocului durerii
Vederi moderne cu privire la geneza și tratamentul șocului durerii Postpartum hemoragie: cauze, tratament, prevenire
Postpartum hemoragie: cauze, tratament, prevenire Șoc generic
Șoc generic Tratamentul HMC hemodinamice acute
Tratamentul HMC hemodinamice acute Sangerarea de la diverticulii a esofagului
Sangerarea de la diverticulii a esofagului Clinica și diagnosticul de șoc traumatic
Clinica și diagnosticul de șoc traumatic Terminologia și clasificarea leziunilor pelvine
Terminologia și clasificarea leziunilor pelvine Mecanismul de încălcare a funcțiilor organismului în pierdere acută de sânge
Mecanismul de încălcare a funcțiilor organismului în pierdere acută de sânge Sangerarea si pierderea de sange in leziuni combatante. În rănile penetrante ale pieptului
Sangerarea si pierderea de sange in leziuni combatante. În rănile penetrante ale pieptului Ajutor cu privire la etapele de evacuare medicală, atunci când pierderea de sânge
Ajutor cu privire la etapele de evacuare medicală, atunci când pierderea de sânge Măsurarea pierderii de sânge
Măsurarea pierderii de sânge Sângerare. Este recomandabil să se facă distincția între sângerare externă, de diagnosticare la…
Sângerare. Este recomandabil să se facă distincția între sângerare externă, de diagnosticare la… Sindromul Mallory-Weiss, în care sursa de hemoragie gastro-intestinală este o fisură, are un tablou…
Sindromul Mallory-Weiss, în care sursa de hemoragie gastro-intestinală este o fisură, are un tablou… Șoc traumatic, reacția grea totală a corpului cu trauma tesut masiv si pierderea de sange.…
Șoc traumatic, reacția grea totală a corpului cu trauma tesut masiv si pierderea de sange.… Sănătate Enciclopedia, boli, medicamente, medic, farmacie, infecție, rezumate, sex, ginecologie,…
Sănătate Enciclopedia, boli, medicamente, medic, farmacie, infecție, rezumate, sex, ginecologie,… Sănătate Enciclopedia, boli, medicamente, medic, farmacie, infecție, rezumate, sex, ginecologie,…
Sănătate Enciclopedia, boli, medicamente, medic, farmacie, infecție, rezumate, sex, ginecologie,… Hematologie-transfuziolog (transfuzii de sânge)
Hematologie-transfuziolog (transfuzii de sânge)
 Tratamentul HMC hemodinamice acute
Tratamentul HMC hemodinamice acute Șoc generic
Șoc generic